想象一下,你是一位试图了解细胞工作原理的生物学家。你怀疑敲除特定基因会改变细胞的状态,也许能将癌细胞转化为良性细胞。你有 20 个不同的基因可以作为目标。
如果你一次测试一个基因,那是 20 次实验。这很容易管理。但生物学很少是线性的;基因之间存在相互作用。一个基因单独作用可能毫无反应,但如果与另一个基因配对,可能对细胞是致命的。为了充分理解这个系统,你需要测试各种组合。
问题就在这里: 组合爆炸 (The Combinatorial Explosion) 。
有 20 个基因,可能的组合数量 (即“全因子”设计) 是 \(2^{20}\),这超过了一百万次实验。在湿实验室 (wet lab) 中,这是不可能的。你需要一种方法来运行可控数量的实验——比如 1,000 次——同时尽可能多地了解这些基因是如何相互作用的。
这正是 Divya Shyamal、Jiaqi Zhang 和 Caroline Uhler 的研究论文 “Probabilistic Factorial Experimental Design for Combinatorial Interventions” 所解决的问题。
在这篇文章中,我们将深入探讨他们提出的框架: 概率因子设计 (Probabilistic Factorial Design) 。 我们将探索为何给治疗分配概率 (剂量) ,而不是手工挑选组合,能提供一种可扩展且具有理论依据的方法,从而无需进行一百万次实验就能学习复杂的相互作用。
设计困境: 全因子 vs. 部分因子
在看新的解决方案之前,让我们先了解一下现状。
- 全因子设计 (Full Factorial Design) : 你测试每一个可能的组合。
- *优点: * 获得所有相互作用的完美数据。
- *缺点: * 数学上无法扩展。实验数量随治疗数量 (\(p\)) 指数增长。
- 部分因子设计 (Fractional Factorial Design) : 你选择特定的组合子集进行测试。
- *优点: * 使用的样本较少。
- *缺点: * 它很僵化。你需要仔细选择运行哪些组合以避免“混叠” (aliasing,即混淆不同的相互作用) 。如果设计错误,你可能会认为基因 A 和基因 B 在相互作用,而实际上是基因 C 在单独起作用。设计这些实验需要大量的先验假设 (例如,“我假设不存在 3 方式相互作用”) 。
本文作者提出了第三种方式,灵感来自于高通量生物筛选 (如 Perturb-seq) 的实际操作方式。他们建议采用概率方法,而不是明确选择“第 1 行接受基因 A 和 B”。
概率框架
核心思想简单而强大。实验者不是为某个单元 (如一个细胞) 分配固定的治疗组合,而是选择一个剂量 (dosage) 向量 \(\mathbf{d} = (d_1, \dots, d_p)\)。
每个 \(d_i\) 代表应用治疗 \(i\) 的概率。对于每个实验单元 \(m\),治疗分配是基于这些概率随机抽取的。
在数学上,令 \(x_{m,i}\) 为治疗 \(i\) 在单元 \(m\) 上的干预状态。它的取值为 1 (应用治疗) 或 -1 (对照/未应用) 。

为什么要这样做?这一点非常巧妙:
- 如果你设置 \(\mathbf{d} \in \{0, 1\}^p\),你就恢复了传统的确定性设计。
- 如果你设置 \(\mathbf{d} \in (0, 1)^p\),你就创建了一个随机设计,随机探索组合空间。
通过调整连续参数 \(\mathbf{d}\),实验者可以控制实验的“重心”,而无需明确枚举每一个组合。
组合结果建模
为了优化设计,我们需要一个世界的数学模型。输入 (治疗) 如何映射到输出 (结果) ?
作者将单元 \(m\) 的结果 \(y_m\) 定义为治疗向量 \(\mathbf{x}_m\) 的函数加上一些噪声:
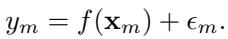
函数 \(f\) 可以是任何东西。然而,为了分析相互作用,作者使用了布尔函数的傅里叶展开 。 虽然“傅里叶”通常让我们想到正弦波,但在二进制输入 (\(\{-1, 1\}\)) 的背景下,傅里叶基函数仅仅是输入的乘积。
对于治疗的任意子集 \(S \subseteq [p]\),基函数为:
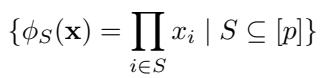
这看起来很抽象,让我们具体一点。
- 如果 \(S = \{1\}\),那么 \(\phi_S(\mathbf{x}) = x_1\)。这测量了治疗 1 的主效应。
- 如果 \(S = \{1, 2\}\),那么 \(\phi_S(\mathbf{x}) = x_1 x_2\)。这测量了治疗 1 和 2 之间的成对相互作用 。
任何函数 \(f\) 都可以写成这些相互作用的加权和:
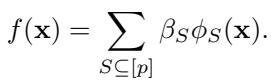
这里,\(\beta_S\) 代表集合 \(S\) 的相互作用强度。如果 \(\beta_{\{1,2\}}\) 很大,意味着基因 1 和 2 有很强的协同作用 (或拮抗作用) 。
与多项式模型的联系
这种傅里叶方法等同于统计学中常用的标准多项式响应面模型。如果你习惯看到像 \(\alpha_{ij} \mathbb{1}_{x_i=x_j=1}\) 这样的相互作用项,它们可以直接映射到傅里叶系数 \(\beta_S\)。
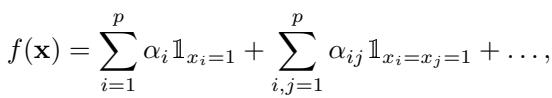
标准系数 (\(\alpha\)) 和傅里叶系数 (\(\beta\)) 之间的关系是线性的:
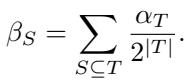
有界相互作用
在现实世界中,我们很少看到 10 个不同的基因以一种无法用低阶效应解释的独特方式同时相互作用。作者假设有界阶相互作用 (Bounded-order interactions) 。 我们假设相互作用仅存在于大小不超过 \(k\) 的范围内 (例如 \(k=2\) 或 \(k=3\)) 。
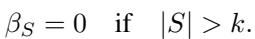
这个假设至关重要,因为它将我们需要估计的参数数量从 \(2^p\) 减少到 \(p\) 的多项式级别,使问题变得可解。
被动设置: “一劳永逸”策略
论文的第一个主要贡献解决了被动 (passive) 设置问题。你有 \(n\) 个样本的预算。你需要在开始时一次性选择剂量向量 \(\mathbf{d}\)。你应该选择什么剂量才能尽可能准确地估计模型系数 \(\boldsymbol{\beta}\)?
为了回答这个问题,我们看看估计量。我们希望从数据观察中恢复 \(\boldsymbol{\beta}\)。设计矩阵 \(\mathcal{X}\) 包含每个样本的傅里叶特征:
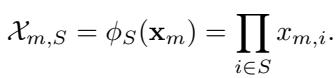
由于我们的设计是随机的,矩阵 \(\mathcal{X}\) 可能是病态的 (某些列可能偶然相关) 。为了处理这个问题,作者使用了截断普通最小二乘法 (Truncated Ordinary Least Squares, OLS) 估计量。本质上,它执行标准的线性回归,但如果矩阵太不稳定 (即特征值太小) ,它会“放弃” (返回零) 以避免巨大的方差。
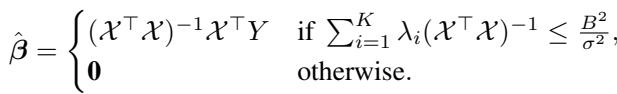
指标: 均方误差
我们希望最小化估计系数 \(\hat{\boldsymbol{\beta}}\) 和真实系数 \(\boldsymbol{\beta}\) 之间的预期均方误差 (MSE)。该误差的理论界限很大程度上取决于矩阵 \(\mathcal{X}^\top \mathcal{X}\) 的特征值 (\(\lambda_i\))。
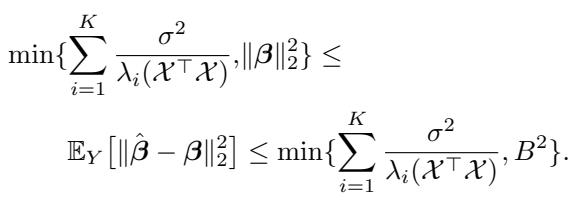
\(\sum \frac{1}{\lambda_i}\) 这一项是关键。在线性回归中,估计量的方差与逆协方差矩阵的迹成正比。 为了最小化误差,我们需要大的特征值。
最优策略
这是论文中一个惊人的结果。在概率设计框架下,对于任何相互作用阶数 \(k\):
最优剂量是 \(\mathbf{d} = (1/2, 1/2, \dots, 1/2)\)。
这意味着基本上就是为每个单元的每个治疗抛一枚公平的硬币。
为什么是 \(1/2\) 最优? 这归结为总体协方差矩阵,记为 \(\Sigma(\mathbf{d})\)。该矩阵的元素由剂量决定:
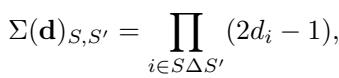
该矩阵的特征值决定了误差。无论 \(\mathbf{d}\) 如何,特征值之和是常数。根据调和平均数的性质 (柯西-施瓦茨不等式) ,当所有特征值相等时,逆特征值之和最小。
当 \(\mathbf{d} = 1/2\) 时,项 \((2d_i - 1)\) 变为 0。这将协方差矩阵 \(\Sigma(\mathbf{d})\) 坍缩为单位矩阵 。 单位矩阵的所有特征值都等于 1。这是回归的完美条件——这意味着你所有的特征 (相互作用) 彼此完全不相关。
作者证明剂量 1/2 在一个非常小的因子范围内是最优的:
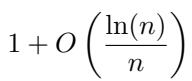
具体来说,误差率随样本量 \(n\) 衰减如下:
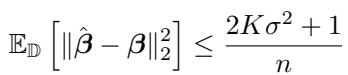
这意味着要估计一个 \(k\) 方式相互作用模型,你需要大约 \(O(k p^{3k} \ln p)\) 个样本。这是多项式级别的,而不是指数级别的,这对于可扩展性来说是一个巨大的胜利。
主动设置: 边做边学
在许多科学场景中,你不会一次性运行所有实验。你会运行一批,分析数据,然后设计下一批。这就是主动学习 (Active Learning) 。
假设我们已经进行了 \(T-1\) 轮实验。我们收集了数据矩阵 \(\mathcal{X}_1, \dots, \mathcal{X}_{T-1}\)。我们希望选择下一轮的剂量 \(\mathbf{d}_T\) 以最小化总误差。
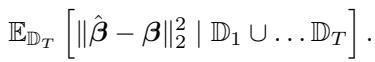
由于我们已经有了数据,我们当前的“信息”由前几轮的格拉姆矩阵 \(\mathcal{X}^\top \mathcal{X}\) 之和表示。我们可能偶然收集到了有偏差的数据,或者第一轮被迫使用了次优剂量。第 \(T\) 轮是我们“修正”协方差结构的机会。
作者推导了一个近似最优的采集函数。我们选择剂量 \(\mathbf{d}_T\) 来最小化合并后协方差 (过去的数据 + 预期的新数据) 的逆特征值:
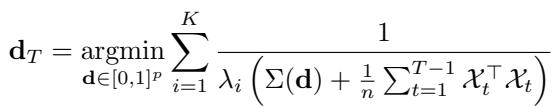
这个公式不能像被动设置那样有闭式解,但它是 \(\mathbf{d}\) 的平滑函数。这意味着我们可以使用数值优化 (如梯度下降或 SLSQP) 来找到下一轮的最佳剂量。
这是一个强大的工具。它允许实验动态地“填补”信息空间中的漏洞。
扩展: 现实世界的约束
论文将此框架扩展到了几个实际场景。
1. 供应有限
如果试剂昂贵,或者同时应用过多治疗会杀死细胞怎么办?我们可能会施加一个约束,即剂量之和不能超过限制 \(L\):
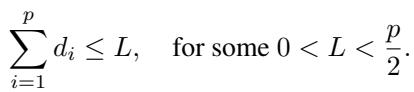
对于简单的加性模型 (\(k=1\)) ,作者证明最优策略是平均分配预算,即对所有治疗设置 \(d_i = L/p\)。对于高阶相互作用,数值优化器 (来自主动设置) 可以遵守此约束并找到最佳解。
2. 异方差噪声
如果不同轮次的实验具有不同的噪声水平 (\(\sigma_t^2\)) 怎么办?也许实验室设备重新校准了,或者使用了不同批次的细胞。优化函数通过按精度 (\(1/\sigma^2\)) 加权协方差矩阵来自然适应这种情况:
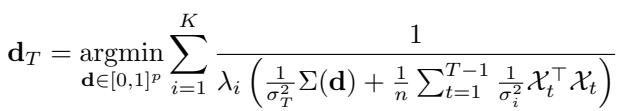
3. 模拟目标分布
有时,你不只是想最小化回归误差。你可能希望你的实验群体模仿自然界中发现的特定组合分布 \(q\)。
作者表明,通过最小化目标分布 \(q\) 与设计分布 \(p_{\mathbf{d}}\) 之间的 KL 散度,最优剂量仅仅是目标分布的边缘概率。
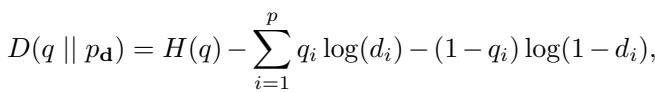
实验验证
理论听起来很可靠,但在实践中有效吗?作者进行了模拟来验证他们的主张。
模拟 1: 1/2 真的是最优的吗?
在这个实验中,他们固定了一个“真实”模型,并尝试使用不同的剂量向量来估计它。他们改变了剂量向量与理论最优值 \(0.5\) 的距离。
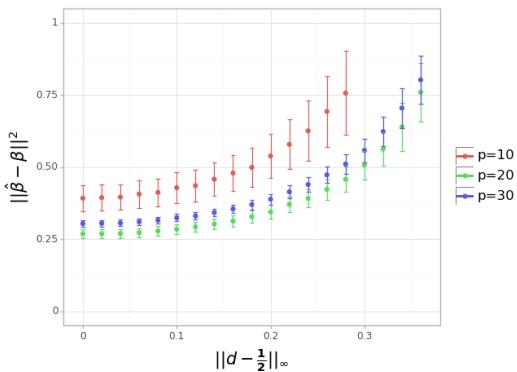
解释: 看图 1。x 轴表示与剂量 0.5 的距离。y 轴是估计误差。当你远离 0.5 时,曲线明显上升。这从经验上证实了定理: “公平抛硬币” (0.5) 能最小化误差。
模拟 2: 均匀剂量
他们还测试了将所有剂量设置为相同的值 \(d\),将 \(d\) 从 0.4 变化到 0.6。
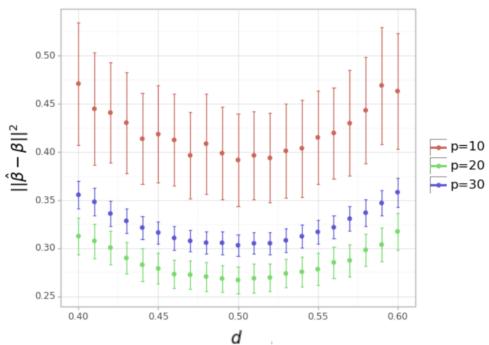
解释: 图 2 显示了一个清晰的“U”形,中心正好在 0.5。即使稍微偏离 (例如到 0.4 或 0.6) 也会增加误差,加强了被动设置中半剂量策略的敏感性和最优性。
模拟 3: 主动 vs. 随机
在这里,他们比较了主动 (Active) 策略 (每轮优化剂量) 与随机 (Random) 策略 (选择随机剂量) 以及固定的半剂量 (Half) 策略。
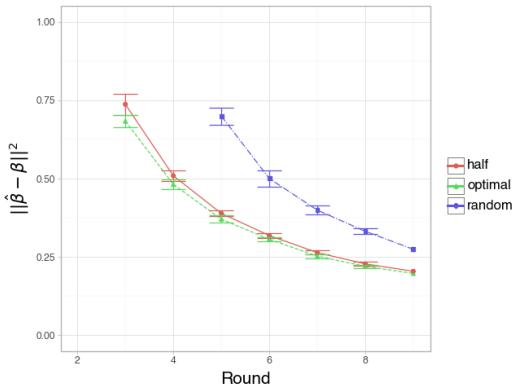
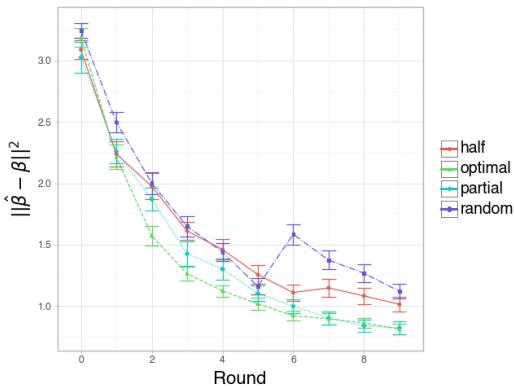
解释:
- 图 3 (大 \(N\)) : 有了足够的样本,“半剂量”策略 (红色) 和“最优”主动策略 (绿色) 表现同样出色,都击败了随机策略 (蓝色) 。这说得通;如果你有足够的数据,被动最优策略很难被击败。
- 图 4 (小 \(N\),高噪声) : 这是有趣的情况。当数据稀缺时, 最优策略 (绿色) 在早期轮次中明显优于其他策略。这表明当实验昂贵 (样本量小) 时,使用主动学习框架计算精确的最优剂量具有显著优势。
模拟 4: 约束优化
最后,他们测试了剂量总和受限的有限供应场景。
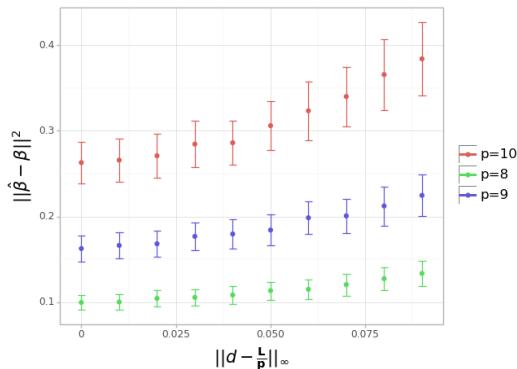
解释: 随着剂量偏离可用预算的均匀分布 (\(L/p\)),误差增加。这证实了即使在约束条件下,平均分配资源通常也是学习相互作用的最佳起始策略。
结论与关键要点
论文 “Probabilistic Factorial Experimental Design for Combinatorial Interventions” 为困扰许多实验科学的问题提供了一个严谨的数学基础: 如何在不测试所有内容的情况下研究复杂的组合。
关键要点:
- 概率设计: 从离散的组合选择转向连续的“剂量”,使设计问题变得可微分且可扩展。
- 1/2 的力量: 在被动 (一次性) 实验中,将每个治疗概率设置为 50% 对于学习任何阶数的相互作用在理论上都是近似最优的。它使特征不相关。
- 主动修正: 如果分轮进行实验,你可以数值优化剂量以修正过去的不平衡或约束,这在样本量较小时特别有价值。
- 灵活性: 该框架自然地处理约束 (预算限制) 和实验噪声的变化。
对于学生和研究人员来说,这项工作弥合了经典实验设计 (可能过于僵化) 与现代高通量能力之间的差距。它表明,有时理解复杂确定性系统的最佳方法是用随机性去探索它。
](https://deep-paper.org/en/paper/2506.03363/images/cover.png)